第Ⅱ章 リンパ腫
Ⅱ リンパ腫
7 末梢性T細胞リンパ腫
(peripheral T-cell lymphoma:PTCL)
総論
WHO分類(2017)では成熟TおよびNK細胞腫瘍として,約30種の疾患単位が記載されている1)。発症頻度はすべての悪性リンパ腫の約7%程度(日本では10%弱)と,稀なリンパ腫病型である2)。末梢性T細胞リンパ腫(peripheral T-cell lymphoma:PTCL)に関する国際共同後方視的観察研究(International T-cell Lymphoma Project)では,欧米ではPTCL・非特定型(PTCL, not otherwise specified:PTCL-NOS),血管免疫芽球性T細胞リンパ腫(angioimmunoblastic T-cell lymphoma:AITL),未分化大細胞リンパ腫(anaplastic large cell lymphoma:ALCL)・ALK陽性およびALCL・ALK陰性の4病型の発症頻度が高いことが報告された3)。本項ではこの4病型について取り扱う。一方,日本ではこの4病型に加えて成人T細胞白血病・リンパ腫(adult T-cell leukemia/lymphoma:ATL),節外性NK/T細胞リンパ腫・鼻型(extranodal NK/T-cell lymphoma, nasal type:ENKL)の頻度が高く,この2病型については本ガイドラインでは別項として扱う。皮膚T細胞リンパ腫については,独自のガイドライン4)が作成されているため,本項では扱わない。
International T-cell Lymphoma Projectで成熟T/NK細胞腫瘍における発症頻度が5%未満の希少病型として,腸症関連T細胞リンパ腫(enteropathy-associated T-cell lymphoma:EATL),原発性皮膚ALCL,肝脾T細胞リンパ腫(hepatosplenic T-cell lymphoma:HSTL),皮下脂肪織炎様T細胞リンパ腫が挙げられる3)。EATLは,WHO分類(2017)ではCeliac病との関連がない病型[WHO分類(2007)でのEATL, typeⅡ]がmonomorphic epitheliotropic intestinal T-cell lymphoma(MEITL)として独立した。HSTLは細胞傷害性T細胞(通常はγδ型)に由来する病型で,著明な肝脾腫を特徴とし,典型的にはリンパ節腫脹を伴わない。MEITLもHSTLも臨床的に進行性であることが多く,CHOP/CHOP類似療法での予後は不良である1)。
また,WHO分類(2017)ではAITLの項に,T濾胞ヘルパー(T follicular helper:TFH)細胞起源節性リンパ腫として,follicular T-cell lymphoma(FTCL)およびNodal PTCL with TFH phenotypeが新たに記載された1)。これらは従来AITLあるいはPTCL-NOSと診断されていたが,TFH由来のT細胞腫瘍として特徴的な遺伝子異常を伴うことが報告され,新たな疾患亜型となった。病型特異的な治療は未確立であり,現時点では従来通りにAITLあるいはPTCL-NOSとして治療される。
病期分類および効果判定規準には,他のリンパ腫病型と同様にLugano分類が用いられる5)。PTCLの大半の病型ではpositron emission tomography(PET)検査において高率に18fluoro-2-deoxyglucose(FDG)の取り込みが認められる “FDG-avid” であるため6),病期診断および効果判定のいずれにおいてもFDG-PET/CT検査が有用である。予後予測モデルとしては国際予後指標(International Prognostic Index:IPI)が有用であり,PTCL-NOSにおいてはPIT(Prognostic Index for PTCL-U)がある。PITでは,年齢>60歳,PS>1,血清LDH値>施設基準値上限,骨髄浸潤あり,の4つの因子が予後不良因子と規定されている7)。これらの予後予測モデルでは,主にCHOP/CHOP類似療法を施行された場合の予後予測性が示されているが,これらのリスクによる治療の層別化は行われていない。
参考文献
1) Swerdlow SH, et al. eds. Mature T- and NK-cell neoplasms. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC; 2017: pp368-71.(テキストブック)
2) Chihara D, et al. Differences in incidence and trends of haematological malignancies in Japan and the United States. Br J Haematol. 2014; 164(4): 536-45.(3iiA)
3) Vose J, et al. International peripheral T-cell and natural killer/T-cell lymphoma study: pathology findings and clinical outcomes. J Clin Oncol. 2008; 26(25): 4124-30.(3iiA)
4) 日本皮膚科学会, 日本皮膚悪性腫瘍学会, 日本皮膚悪性腫瘍診療ガイドライン改訂委員会 皮膚リンパ腫診療ガイドライングループ. 皮膚悪性腫瘍ガイドライン第3 版 皮膚リンパ腫診療ガイドライン 2020. 日皮会誌 . 2020; 130(6): 1347-423.(ガイドライン)
5) Cheson BD, et al. Recommendations for initial evaluation, staging, and response assessment of Hodgkin and non-Hodgkin lymphoma: the Lugano classification. J Clin Oncol. 2014; 32(27): 3059-68.(レビュー)
6) Barrington SF, et al. Role of imaging in the staging and response assessment of lymphoma: consensus of the International Conference on Malignant Lymphomas Imaging Working Group. J Clin Oncol. 2014; 32(27): 3048-58.(3iiiDiii)
7) Gallamini A, et al. Peripheral T-cell lymphoma unspecified(PTCL-U): a new prognostic model from a retrospective multicentric clinical study. Blood. 2004; 103(7): 2474-9.(3iiA)
アルゴリズム
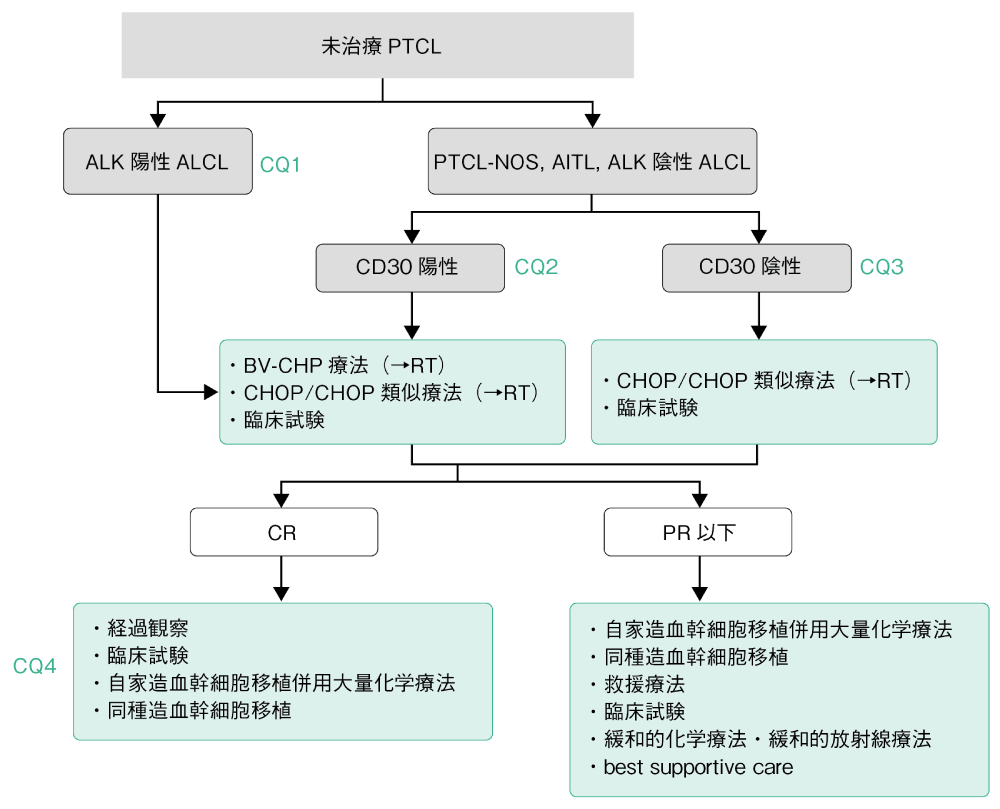
総論で記載した通り,本項ではPTCL-NOS,AITL,ALK陽性ALCL,ALK陰性ALCLの4病型について取り扱う。PTCLは無治療で月単位の病勢進行を示すアグレッシブリンパ腫(中高悪性度リンパ腫)であり,診断後には原則としてすべての患者が治療対象となる。かつては,びまん性大細胞型B細胞リンパ腫(diffuse large B-cell lymphoma:DLBCL)などの他のアグレッシブリンパ腫と同様な治療開発が行われてきたが,抗CD20モノクローナル抗体であるリツキシマブ(R)の臨床導入によってB細胞リンパ腫とPTCLとの治療開発は分けられた。R臨床導入以前の国際共同後方視的研究において,ALCLを除くすべてのPTCLの予後はDLBCLと比して不良であることが示された1)。International T-cell Lymphoma Projectにおいて,CHOP/CHOP類似療法が行われたPTCLでは,ALK陽性ALCLは最も予後良好(5年OS 70%)で,PTCL-NOSとAITLとは同程度に予後が悪く(5年OS 32%),ALK陰性ALCLはその中間程度の予後(5年OS 49%)であることが報告された2)。このため,PTCLにおいてはALK陽性ALCLと,その他の病型との2群に分けて治療方針が検討されてきた。
ALK陽性ALCLは上記の通りPTCLにおいて比較的予後良好とされる。ALCLでは腫瘍細胞にCD30が高発現している。CD30陽性PTCLに対するCHOP療法とブレンツキシマブ ベドチン(BV)併用CHP(BV-CHP)療法との第Ⅲ相試験(ECHELON-2)では,BV-CHP療法がCHOP療法に比べてPFSおよびOSで有意に優れていた3)。ECHELON-2試験で対象となったIPI 2以上のALK陽性ALCLではBV-CHP療法が推奨される(CQ1)。IPI 0~1のALK陽性ALCLでは従来通りにCHOP/CHOP類似療法が推奨されるが,BV-CHP療法も選択可能である(CQ1)。PTCL-NOS,AITL,ALK陰性ALCLにおいても,CD30陽性であればECHELON-2試験の結果に従ってBV-CHP療法が推奨される(CQ2)。ただし,ECHELON-2試験の病型別サブグループ解析では,PTCL-NOSとAITLにおいてBV併用の良好性は認められなかったため,CD30陽性であっても従来通りCHOP/CHOP類似療法も選択可能である(CQ2)。一方,CD30陰性であれば従来通りに最も多くの治療実績が報告されているCHOP/CHOP類似療法が推奨される(ALK陰性ALCLは診断規準上CD30陽性であるため,CQ3の対象には含めない)。ただし,その治療成績は十分でなく,治療成績向上を目指した標準治療開発のために臨床試験への参加が推奨される(CQ3)。限局期の場合は局所放射線療法の追加も選択肢となる(CQ1~3)。初発PTCLの初回CR時には経過観察が推奨される。初回CRに引き続いて自家造血幹細胞移植併用大量化学療法(自家移植)を施行する意義は不明であり,一般診療での施行は推奨されず,臨床試験として実施することが望ましい(CQ4)。初回治療後のPR以下の場合には,自家移植,同種造血幹細胞移植(同種移植),救援療法(多剤併用化学療法,単剤療法)などが一般診療における主な選択肢であるが,これらの治療選択に関するエビデンスは乏しい。このため,臨床試験への参加も推奨される。全身状態不良,臓器障害あるいは患者希望などにより積極的な抗腫瘍療法の適応とならない場合もある(緩和的化学療法・緩和的放射線療法,best supportive care:BSC)。
参考文献
1) A clinical evaluation of the International Lymphoma Study Group classification of non-Hodgkin’s lymphoma. The Non-Hodgkin’s Lymphoma Classification Project. Blood. 1997; 89(11): 3909-18.(3iiA)
2) Vose J, et al. International peripheral T-cell and natural killer/T-cell lymphoma study: pathology findings and clinical outcomes. J Clin Oncol. 2008; 26(25): 4124-30.(3iiA)
3) Horwitz S, et al. Brentuximab vedotin with chemotherapy for CD30-positive peripheral T-cell lymphoma(ECHELON-2): a global, double-blind, randomized, phase 3 trial. Lancet. 2019; 393(10168): 229-40.(1iDiii/1iA)
CQ1 未治療ALK陽性ALCLにはどのような治療が勧められるか
- 推奨グレード
- カテゴリー1
ブレンツキシマブ ベドチン併用CHP(BV-CHP)療法が推奨される。
解説
ALK陽性ALCLは,代表的にはt(2;5)(p23:q35)の染色体転座を有し,nucleophosmin(NPM1)遺伝子とALK遺伝子とが融合したキメラ遺伝子が病態に関与する病型である。その診断には腫瘍細胞にCD30抗原発現の確認が必要である。ALK陽性ALCLはすべての非ホジキンリンパ腫のうち3%であるが,小児に発症するリンパ腫では10~20%と頻度が高くなる1)。患者の多くは,進行期,IPI 2以上である。CHOP/CHOP類似療法により5年OS 70%と報告されている2,3)。IPIリスク数による5年OSは,0~1:90%,2:68%,3:23%,4:33%と,特に低リスク群の予後は良好である3)。限局期では,他のアグレッシブリンパ腫と同様に,CHOP/CHOP類似療法短期コース後に放射線治療を追加することも治療選択肢となる。
ブレンツキシマブ ベドチン(BV)はキメラ型抗CD30モノクローナル抗体に微小管阻害薬であるmonomethyl auristatin E(MMAE)を酵素切断可能なリンカーによって結合させた抗体薬物複合体である。ALK陽性ALCLを含むCD30陽性PTCLに対するCHOP療法とBV併用CHP(BV-CHP)療法との第Ⅲ相試験(ECHELON-2)では,BV-CHP療法(6~8コース)がCHOP療法(6~8コース)に比してPFSおよびOSで有意に優れていた4)。病型別のサブグループ解析では,ALK陽性ALCLにおいてPFSでハザード比 0.29(95%CI 0.11-0.79),OSでハザード比 0.38(95%CI 0.12-1.22)とBV併用の良好な傾向を認めた。ECHELON-2試験で対象となったIPI 2以上のALK陽性ALCLではBV-CHP療法が推奨される。IPI 0~1のALK陽性ALCLに対してもBV-CHP療法が推奨されるが,CHOP/CHOP類似療法も選択可能である。ECHELON-2試験では予め計画された地固め的な局所放射線療法の施行が許容されていたが,限局期に対してBV-CHP療法の施行コースを短縮して局所放射線療法を追加する治療スケジュールに関するエビデンスはない。
参考文献
1) Swerdlow SH, et al. eds. Mature T- and NK-cell neoplasms. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC; 2017: pp368-71.(テキストブック)
2) Vose J, et al. International peripheral T-cell and natural killer/T-cell lymphoma study: pathology findings and clinical outcomes. J Clin Oncol. 2008; 26(25): 4124-30.(3iiA)
3) Savage KJ, et al. ALK- anaplastic large-cell lymphoma is clinically and immunophenotypically different from both ALK+ ALCL and peripheral T-cell lymphoma, not otherwise specified: report from the International Peripheral T-Cell Lymphoma Project. Blood. 2008; 111(12): 5496-504.(3iiA)
4) Horwitz S, et al. Brentuximab vedotin with chemotherapy for CD30-positive peripheral T-cell lymphoma(ECHELON-2): a global, double-blind, randomized, phase 3 trial. Lancet. 2019; 393(10168): 229-40. (1iDiii/1iA)
CQ2 未治療でCD30陽性のPTCL-NOS, AITL, ALK陰性ALCLにはどのような治療が勧められるか
- 推奨グレード
- カテゴリー1
ブレンツキシマブ ベドチン併用CHP(BV-CHP)療法が推奨される。
解説
抗CD20モノクローナル抗体であるリツキシマブ(R)が臨床導入される以前には,PTCLもアグレッシブリンパ腫として,DLBCLなどの他のアグレッシブリンパ腫病型とともに臨床試験の対象として治療開発が行われていた。米国で行われた,PTCLを含むアグレッシブリンパ腫を対象としたCHOP療法と強力な化学療法レジメンとの4群ランダム化比較試験の結果1),CHOP療法が標準治療と位置付けられた。この結果を受けて,PTCLの標準治療もCHOP療法となった。限局期では,他のアグレッシブリンパ腫と同様に,CHOP/CHOP類似療法短期コース後に放射線治療を追加することも治療選択肢となる。
CD30抗原は,tumor necrosis factor受容体ファミリーに属する膜貫通型受容体の糖蛋白質である。正常組織においては活性化リンパ球や一部の好酸球にのみ発現していることから,CD30抗原は腫瘍特異抗原と考えられている。PTCLの各病型における,免疫組織化学染色によるCD30陽性率はPTCL-NOSで58%,AITLで63%との報告があるが,強陽性率は5~20%程度である。一方,ALK陰性ALCLは定義上,腫瘍細胞にCD30抗原発現が必須であり陽性率は100%かつ強陽性である2)。ブレンツキシマブ ベドチン(BV)はキメラ型抗CD30モノクローナル抗体に微小管阻害薬であるmonomethyl auristatin E(MMAE)を酵素切断可能なリンカーによって結合させた抗体薬物複合体である。ALK陽性ALCLを含むCD30陽性PTCLに対するCHOP療法とBV併用CHP(BV-CHP)療法との第Ⅲ相試験(ECHELON-2)では,BV-CHP療法がCHOP療法に比べてPFSおよびOSで有意に優れていた3)。登録された全患者のうち,ALCLが約70%を占めた。PFSおよびOSの病型別のサブグループ解析では,ALK陰性ALCLにおいてBV併用が良好であったが,PTCL-NOSおよびAITLではBV併用による良好な傾向は認められなかった3)。ECHELON-2試験の5年フォローアップデータでも同様の結果であった4)。ECHELON-2試験としては主要評価項目のPFSおよび副次的評価項目のOSでBV-CHP療法の優位性が示されたため,未治療CD30陽性PTCLに対する初回治療としてBV-CHP療法が標準治療と結論される。ただしALCL以外の病型に対するBV-CHP療法の臨床的適応については検討の余地が残る。このため,PTCL-NOSとAITLにおいてはCHOP/CHOP類似療法の選択も妥当である。
ECHELON-2試験では予め計画された地固め的な局所放射線療法の施行が許容されていたが,限局期に対してBV-CHP療法の施行コースを短縮して局所放射線療法を追加する治療スケジュールに関するエビデンスはない。
参考文献
1) Fisher RI, et al. Comparison of a standard regimen(CHOP)with three intensive chemotherapy regimens for advanced non-Hodgkin’s lymphoma. N Engl J Med. 1993; 328(14): 1002-6.(1iiA)
2) Bossard C, et al. Immunohistochemistry as a valuable tool to assess CD30 expression in peripheral T-cell lymphomas: high correlation with mRNA levels. Blood. 2014; 124(19): 2983-6.
3) Horwitz S, et al. Brentuximab vedotin with chemotherapy for CD30-positive peripheral T-cell lymphoma(ECHELON-2): a global, double-blind, randomized, phase 3 trial. Lancet. 2019; 393(10168): 229-40.(1iDiii/1iA)
4) Horwitz S, et al. The ECHELON-2 Trial: 5-year results of a randomized, phase III study of brentuximab vedotin with chemotherapy for CD30-positive peripheral T-cell lymphoma. Ann Oncol. 2022; 33(3): 288-98.(1iDiii/1iA)
CQ3 未治療でCD30陰性のPTCL-NOS,AITLにはどのような治療が勧められるか
- 推奨グレード
- カテゴリー2A
CHOP/CHOP類似療法が推奨される。ただし,標準治療は確立しておらず,臨床試験への参加が推奨される。
解説
抗CD20モノクローナル抗体であるリツキシマブ(R)が臨床導入される以前には,PTCLもアグレッシブリンパ腫として,DLBCLなどの他のアグレッシブリンパ腫病型とともに臨床試験の対象として治療開発が行われていた。米国で行われた,PTCLを含むアグレッシブリンパ腫を対象としたCHOP療法(CPA, DXR, VCR, PSL)と強力な化学療法レジメンとの4群ランダム化比較試験の結果1),CHOP療法が標準治療と位置付けられた。この結果を受けて,PTCLの標準治療もCHOP療法となった。限局期では,他のアグレッシブリンパ腫と同様に,CHOP/CHOP類似療法短期コース後に放射線治療を追加することも治療選択肢となる。
しかし,R臨床導入以前の国内外の後方視的研究あるいは国内臨床試験グループの併合解析によって,ALCLを除くすべてのPTCLの予後はDLBCLと比して不良であることが報告された2,3)。こうしたことから,PTCLの治療成績向上を目的として,CHOP療法を基軸とした治療レジメンが検討されてきた。ドイツの臨床試験グループで,アグレッシブリンパ腫(PTCLは全体の14%)に対してCHOP療法と,CHOP療法にエトポシドを追加したCHOEP療法(CPA, DXR, VCR, ETP, PSL)とのランダム化比較試験が行われた。PTCLのサブグループ解析においてCHOEP療法がEFSで優れたものの,病型別ではALK陽性ALCLを除くALK陰性ALCL,PTCL-U,AITLでCHOEP療法の優位性が認められなかった4)。また,国内ではDA-EPOCH療法(ETP, PSL, VCR, CPA, DXR)の第Ⅱ相試験5)が行われたが,有効性においてCHOP療法との優位性は不明である。
以上から,未治療でCD30陰性のPTCL-NOS,AITL(なお,ALK陰性ALCLはCD30陽性が診断上必須であるため,本CQの対象とならない)における標準治療は未確立であるため臨床試験への参加が推奨されるが,一般診療ではこれまでの治療実績の観点からCHOP/CHOP類似療法が推奨される。
参考文献
1) Fisher RI, et al. Comparison of a standard regimen(CHOP)with three intensive chemotherapy regimens for advanced non-Hodgkin’s lymphoma. N Engl J Med. 1993; 328(14): 1002-6.(1iiA)
2) A clinical evaluation of the International Lymphoma Study Group classification of non-Hodgkin’s lymphoma. The Non-Hodgkin’s Lymphoma Classification Project. Blood. 1997; 89(11): 3909-18.(3iiA)
3) Watanabe T, et al. Pretreatment total serum protein is a significant prognostic factor for the outcome of patients with peripheral T/ natural killer-cell lymphoma. Leuk Lymphoma. 2010; 51(5): 813-21.(3iiA)
4) Schmitz N, et al. Treatment and prognosis of mature T-cell and NK-cell lymphoma: an analysis of patients with T-cell lymphoma treated in studies of the German High-Grade Non-Hodgkin Lymphoma Study Group. Blood. 2010; 116(18): 3418-25.(3iiiA)
5) Maeda Y, et al. Dose-adjusted EPOCH chemotherapy for untreated peripheral T-cell lymphomas: a multicenter phase II trial of West-JHOG PTCL0707. Haematologica. 2017; 102(12): 2097-103.(3iiiDiv)
CQ4 初発進行期PTCL-NOS, AITL, ALK陰性ALCLの化学療法後CR患者におて地固め療法としての自家造血幹細胞移植併用大量化学療法は勧められるか
- 推奨グレード
- カテゴリー2A
初発進行期PTCL-NOS, AITL, ALK陰性ALCLの化学療法後CR患者における自家造血幹細胞移植併用大量化学療法は,一般診療としての実施は推奨されない。実施する場合は臨床試験として行うことが望ましい。
解説
International T-cell Lymphoma Projectにおいて,CHOP/CHOP類似療法が行われたPTCLでは,ALK陽性ALCLは最も予後良好(5年OS 70%)で,PTCL-NOSとAITLとは同程度に予後が悪く(5年OS 32%),ALK陰性ALCLはその中間程度の予後(5年OS 49%)であることが報告された1)。その治療成績は不十分であり,予後改善を目指して初回奏効期での自家造血幹細胞移植併用大量化学療法(自家移植)が検討された。初回導入化学療法としてCHOP療法を施行し,PR以上の奏効が得られれば引き続き自家移植を行う設定の第II相試験において,自家移植が施行された患者の3年OSは71%と良好であったが,自家移植未施行の患者では11%であった2)。ただし,本試験はランダム化比較試験でなく,34%の患者が初回治療抵抗性あるいは導入化学療法後の病勢進行を主な理由として自家移植を施行できなかったため,自家移植が実施された(実施できた)患者の予後が良好であったことは選択バイアスが除外できないことに留意すべきである。また,患者全体の3~5年PFSは36~44%と長期の治療成績は不十分である2,3)。さらに,複数の後方視的研究で,CHOP/CHOP類似療法でCRとなったPTCL患者に対する自家移植の意義は明らかでないと報告されている4-6)。一方で,米国の前方視的観察研究では,初発PTCLのうち進行期や骨髄浸潤などを有する高リスク患者では,CHOP/CHOP類似療法でCR後の自家移植が予後を改善する可能性が報告されている7)。CD30陽性PTCLに対するCHOP療法とBV-CHP療法のランダム化比較試験であるECHELON-2試験では,導入化学療法で奏効が得られた患者において予め計画されている場合に,引き続く地固め療法としての自家移植の施行が許容されていた。全体で37%(170例)の患者で予め自家移植が計画された8)。結果として19%(88例)が地固め療法としての自家移植を施行され9),BV-CHP療法でCRに至った患者における自家移植が有効である可能性が示唆された10)。このように,一部のPTCL患者では導入療法に引き続く自家移植の施行が有用な可能性があり,また欧米の一部では一般診療として自家移植が実施されている。ただし,初回治療後のCR患者に対する自家移植の意義を検証するランダム化比較試験は実施されておらず,これを積極的に推奨できるエビデンスはない。
以上より,初回治療としてCHOP/CHOP類似療法でCRとなった患者に対する引き続く自家移植を一般診療で実施することは推奨されず,臨床試験での施行が望ましい。
参考文献
1) Vose J, et al. International peripheral T-cell and natural killer/T-cell lymphoma study: pathology findings and clinical outcomes. J Clin Oncol. 2008; 26(25): 4124-30.(3iiA)
2) Reimer P, et al. Autologous stem-cell transplantation as first-line therapy in peripheral T-cell lymphomas: results of a prospective multicenter study. J Clin Oncol. 2009; 27(1): 106-13.(3iiiA)
3) d’Amore F, et al. Up-front autologous stem-cell transplantation in peripheral T-cell lymphoma: NLG-T-01. J Clin Oncol. 2012; 30(25): 3093-9.(3iiA)
4) Abramson JS, et al. Peripheral T-cell lymphomas in a large US multicenter cohort: prognostication in the modern era including impact of frontline therapy. Ann Oncol. 2014; 25(11): 2211-7.(3iiA)
5) Kitahara H, et al. Prognosis of patients with peripheral T cell lymphoma who achieve complete response after CHOP/CHOP-like chemotherapy without autologous stem cell transplantation as an initial treatment. Ann Hematol. 2017; 96(3): 411-20.(3iiA)
6) Fossard G, et al. Role of up-front autologous stem-cell transplantation in peripheral T-cell lymphoma for patients in response after induction: an analysis of patients from LYSA centers. Ann Oncol. 2018; 29(3): 715-23.
7) Park SI, et al. The role of autologous stem cell transplantation in patients with nodal peripheral T-cell lymphomas in first complete remission: Report from COMPLETE, a prospective, multicenter cohort study. Cancer. 2019; 125(9): 1507-17.(3iiA)
8) Horwitz S, et al. Brentuximab vedotin with chemotherapy for CD30-positive peripheral T-cell lymphoma(ECHELON-2): a global, double-blind, randomized, phase 3 trial. Lancet. 2019; 393(10168): 229-40.(1iDiii/1iA)
9) Horwitz S, et al. The ECHELON-2 Trial: 5-year results of a randomized, phase III study of brentuximab vedotin with chemotherapy for CD30-positive peripheral T-cell lymphoma. Ann Oncol. 2022; 33(3): 288-98.(1iDiii/1iA)
10)Savage KJ, et al. Role of stem cell transplant in CD30+ PTCL following frontline brentuximab vedotin plus CHP or CHOP in ECHELON-2. Blood Adv. 2022; 6(19): 5550-55.(1iDiii/2Diii)

