第Ⅱ章 リンパ腫
Ⅱ リンパ腫
4 マントル細胞リンパ腫(mantle cell lymphoma:MCL)
総論
リンパ節濾胞のマントル層(暗殻)を構成するB細胞と同じ細胞表面形質を有する腫瘍である。免疫組織学的にはCD5とcyclin D1およびSOX11が陽性で,分子遺伝学的には95%以上が染色体転座t(11;14)(q13;q32)に伴うBCL-1(CCND1)遺伝子再構成を有する独立した疾患単位である1)。わが国での発症頻度は,全悪性リンパ腫の3%程度である2)。発症年齢中央値は60歳代半ばで男性に多い1,3)。約90%は初発時に病期Ⅲ,Ⅳの進行期で,表在リンパ節腫大以外に70%程度は節外病変を有し,骨髄浸潤は半数以上,脾腫は30%以上,消化管浸潤も30%以上に認められる3)。免疫組織化学染色ではcyclin D1陰性例が15%程度存在し,cyclin D1陽性例に比べ予後良好と報告されている4)。SOX11は,cyclin D1陰性例も大半は陽性となり診断に有用である5)。WHO分類(2017)では,分子亜型として新たにMCL,leukemic,non-nodal typeが記載された。これは脾辺縁帯リンパ腫に類似した病態と比較的インドレントな臨床経過を特徴とする1)。また,従来in situ MCLと記載された初期病変は,in situ mantle-cell “neoplasia”として治療適応外病変と位置付けられた1)。MCLの病期分類には,他の非ホジキンリンパ腫と同様にAnn Arbor分類が用いられる。予後予測モデルとして,国際予後指標(International Prognostic Index:IPI)とは別に,年齢,Performance Status(PS),血清LD,末梢血白血球数の4因子について配点を規定し,総点数により予後をlow,intermediate,highの3群に層別するsimplified MCL International Prognostic Index(MIPI)が提唱され,IPIより予後予測能が高いことが示されている6)。さらに,Ki-67免疫染色陽性率(MIB-1 index)はMIPIの4因子とは異なる独立した予後因子であり,Ki-67免疫染色陽性率を加えたMIPIbも提唱されている6,7)。また,リツキシマブ導入以降では年齢,PS,骨髄浸潤,末梢血白血球数,血清LD,血清アルブミンの6因子を用い,予後をlow,low-intermediate,high-intermediate,highの4群に層別するrevised MIPIも新たに提案されている3)。これらは一般臨床にはあまり用いられていないが,臨床研究の解析には広く導入されている。最近では,遺伝子異常が予後に関わるとの報告がなされており,そのなかでMIPI-cをベースにTP53,KMT2Dの各遺伝子異常を予後因子に加えた,MIPI-genetic(MIPI-g)も提唱されるが8),こちらも一般臨床では用いられておらず,それによる治療層別は今後の課題である。なお,MCLにおいても中枢神経系(CNS)再発が少なからず認められる。Ki-67免疫染色高陽性率やblastoid variantなどCNS浸潤リスク9,10)を有する例ではCNS再発予防に留意する必要があるが,推奨されるCNS予防治療法は確立していない。
参考文献
1) Swerdlow SH, et al. Mantle cell lymphoma. Swerdlow SH, et al. eds. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC; 2017: pp285-90.(テキストブック)
2) Lymphoma Study Group of Japanese Pathologist. The world health organization classification of malignant lymphomas in Japan. incidence of recently recognized entities. Pathol Int. 2000; 50(9): 696-702.
3) Chihara D, et al. Prognostic model for mantle cell lymphoma in the rituximab era: a nationwide study in Japan. Br J Haematol. 2015; 170(5): 657-68.
4) Yatabe Y, et al. Significance of cyclin D1 overexpression for the diagnosis of mantle cell lymphoma: a clinicopathologic comparison of cyclin D1-positive MCL and cyclin D1-negative MCL-like B-cell lymphoma. Blood. 2000; 95(7): 2253-61.(3iiiA)
5) Mozos A, et al. SOX11 expression in highly specific for mantle cell lymphoma and identifies cyclin D1-negative subtpe. Haematologica. 2009; 94(11): 1555-62.
6) Hoster E, et al. A new prognostic index(MIPI)for patients with advanced-stage mantle cell lymphoma. Blood. 2008; 111(2): 558-65.
7) Gressin R, et al. Evaluation of the(R)VAD+C regimen for the treatment of newly diagnosed mantle cell lymphoma. Combined results of two prospective phase II trials from the French GOELAMS group. Haematologica. 2010; 95(8): 1350-57.(3iiiDiv)
8) Ferrero S, et al. KMT2D mutations and TP53 disruptions are poor prognostic biomarkers in mantle cell lymphoma receiving high-dose therapy: a FIL study. Haematologica. 2020; 105(6): 1604-12.(3iiiDiv)
9) Chihara D, et al. Ki-67 is a strong predictor of central nervous system relapse in patients with mantle cell lymphoma(MCL). Ann Oncol 2015; 26(5): 966-73.(3iiiDiv)
10)Cheah CY, et al. Central nervous system involvement in mantle cell lymphoma: clinical features, prognostic factors and outcomes from the European Mantle Cell Lymphoma Network. Ann Oncol 2013; 24(8): 2119-23.(3iiiDiv)
アルゴリズム
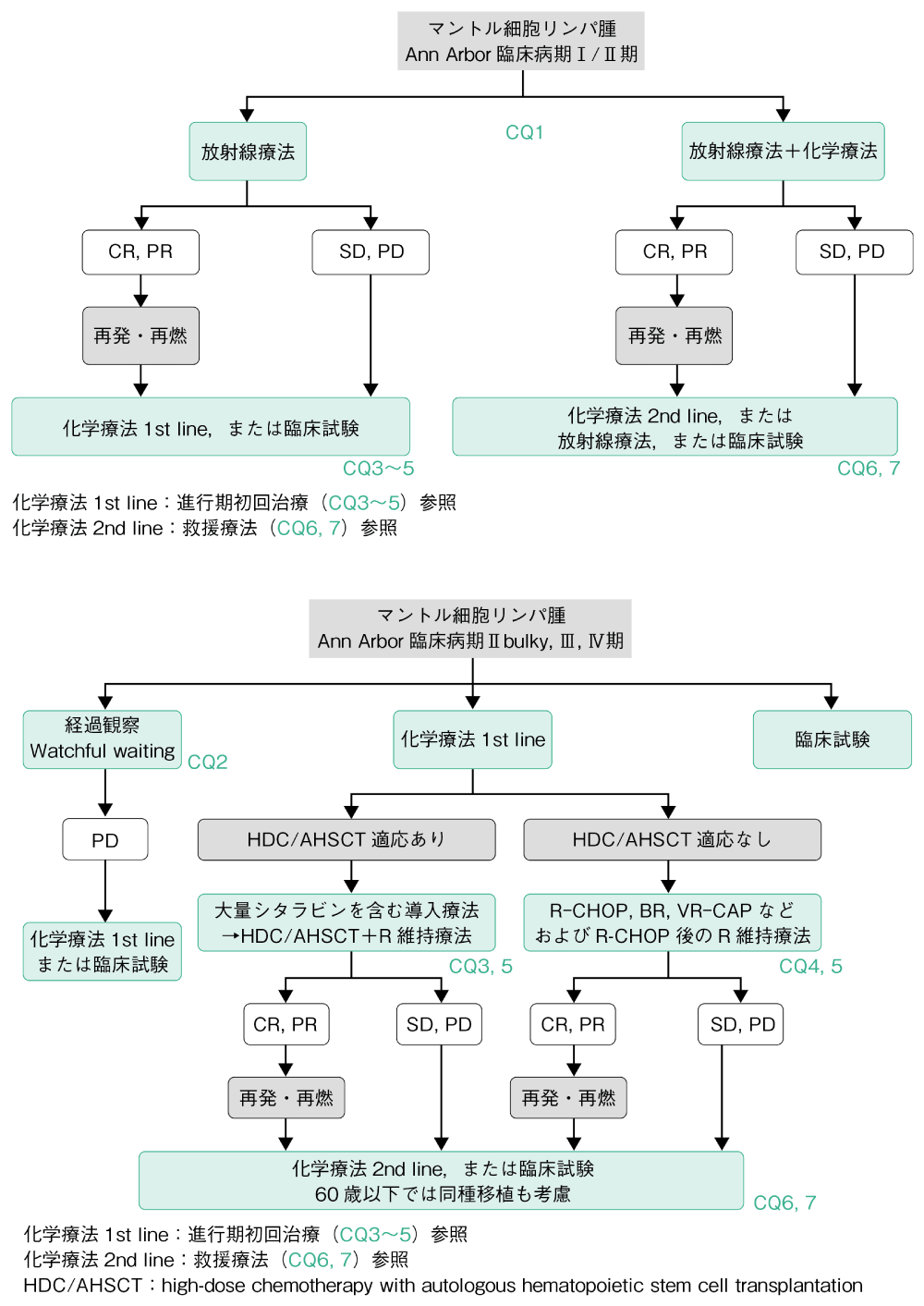
MCLは標準治療が確立しておらず,現在も精力的に臨床試験が進められている。本項では日常診療として実施可能な治療をもとにアルゴリズムを作成した。
限局期ではinvolved site radiation therapy(ISRT)±化学療法群と,化学療法単独または経過観察群との治療成績の比較から,ISRT単独もしくはISRTと化学療法との併用が推奨される(CQ1)。進行期の治療の原則は多剤併用化学療法とリツキシマブ(R)との併用療法である。MCL,leukemic,non-nodal typeなど限られた症例ではあるが,極めて緩徐な臨床経過を示す群がある。これらはインドレントMCLとして,濾胞性リンパ腫などの低悪性度B細胞リンパ腫と同様に無治療で経過観察することが可能であるが,診断時にこのような症例を見出す方法は確立していない(CQ2)。進行期MCLに対しアグレッシブリンパ腫の標準的化学療法であるCHOP療法(CPA,DXR,VCR,PSL)またはその類似療法単独での長期治療成績は不良である。これらにRを併用することでCR割合が改善し良好な分子生物学的奏効も得られるが,長期PFSの改善は十分ではない。このため,65歳以下の症例にはRと大量シタラビンを組み込んだ強化型化学療法を実施し,奏効例には可能であれば第一奏効期に地固め療法として自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)を行うことが推奨される(CQ3)。自家移植後にR維持療法を追加することが推奨される。しかし,そのエビデンスとなった臨床試験のR投与期間は本邦の承認期間とは異なる点に留意が必要である(CQ5)。一方,66歳以上あるいは強化型化学療法の適用が困難な場合は,R-CHOP療法および奏効例にはその後のR維持療法,BR療法(BEN,R),VR-CAP療法(BOR,R,CPA,DXR,PSL),I+BR療法(IBT,BEN,R)などが推奨される(CQ4,5)。初回治療に際しては臨床病態,病理組織学所見などを詳細に検討し,患者個々に最も有用性が高いと考えられる治療法を選択する必要がある。再発・初回治療抵抗例にはベンダムスチン,ボルテゾミブ,多剤併用療法に加え,共有結合型ブルトンキナーゼ(BTK)阻害薬イブルチニブ、非共有結合型BTK阻害薬ピルトブルチニブが導入され、が導入され良好な治療成績が報告されている(CQ6)。既存の薬物療法の治療効果が乏しい場合やTP53変異を有する予後不良MCLの場合,NRMが高いが持続的寛解到達の可能性があり,同種移植は選択肢の一つとなる(CQ7)。標準治療が確立していないMCLでは,新規治療薬の臨床試験への参加も選択肢となる。これら救援療法が不応・不適応の場合は,緩和的なISRTの適用も考慮される。
CQ1 限局期MCLの初回治療としてどのような治療が勧められるか
- 推奨グレード
- カテゴリー2B
慎重に判断された限局期MCLには,combined-modality therapyまたは放射線治療単独が推奨される。
解説
限局期の治療を選択するには,PET/CT,上下部内視鏡などにより全身を検索し限局期であることを慎重に判断する必要がある。
限局期症例に対する放射線治療(RT)を検討した後方視的解析では,2年,5年PFSは65%と46%,2年OSは86%と70%で,年齢とRTの有無がPFSの有意な予後因子であった1)。また,病期Ⅰ・Ⅱ期のMCL 675例の後方視的検討でも,OSはRT群で有意に延長した(103カ月 vs. no-RT群66カ月)2)。限局期MCLに対する化学療法により,3.5年RFSは59.1%で,推定5年OS・RFSは80.4%・37.6%であった3)。
化学療法と放射線照射を組み合わせたcombined-modality therapy(CMT)を検討した単施設での後方視的解析では,病期Ⅰ期では8例中2例,病期Ⅱ期では13例中7例に照射領域外の再発がみられた。限局期MCLにCMTは有用であるが,病期Ⅱ期では照射領域外の再発が多い。Ⅱ期症例では放射線療法の適応を慎重に考える必要がある4)。
一方で,病期Ⅰ・Ⅱ期MCLに対してRT,化学療法,またはその両方(CMT)を実施した2,539例の後方視的解析では,CMT群の生存期間が有意に延長しており(CMT群の生存期間中央値104.8カ月・3年OS 79.8% vs. RT群75.7カ月・72.8%,化学療法群67.6カ月・67.8%),RT群と化学療法群での差は認められなかった.多変量解析ではCMTが有意に死亡リスクを低下させた5)。
以上から,比較試験はないものの,限局期MCLに対しては,RTの有用性が示唆されており,CMTまたはRTが推奨される。
参考文献
1) Leitch HA, et al. Limited-stage mantle-cell lymphoma. Ann Oncol. 2003; 14(10): 1555-61.(3iiDiii)
2) Guru Murthy GS, et al. Effect of radiotherapy on the survival of patients with stage I and stage II mantle cell lymphoma: analysis of the Surveillance, Epidemiology and End Results database. Clin Lymphoma Myeloma Leuk. 2014; 14 Suppl: S90-5.(3iA)
3) Jo JC, et al. Clinical features and treatment outcomes of limited-stage mantle cell lymphoma: Consortium for Improving Survival of Lymphoma report. Ann Hematol. 2020; 99(2): 223-8.(3iiiDiv)
4) Bernard M, et al. Limited-stage mantle cell lymphoma: treatment outcomes at the Princess Margaret Hospital. Leuk Lymphoma. 2013; 54(2): 261-7.(3iiA)
5) Gill BS, et al. Management Trends and Outcomes for Stage I to II Mantle Cell Lymphoma Using the National Cancer Data Base: Ascertaining the Ideal Treatment Paradigm. Int J Radiat Oncol Biol Phys. 2015; 93(3): 668-76.(3iA)
CQ2 初発MCLに対する初回治療として無治療経過観察は勧められるか
- 推奨グレード
- カテゴリー2B
MCLの一部は緩徐な経過を呈する。診断時の情報でこのような症例を同定することは困難であるが,緩徐な経過を呈する症例では,無治療経過観察も選択肢として推奨される。
解説
MCLの一部は緩徐な経過を呈し,無治療経過観察も選択肢となる。単施設の97例の後方視的な解析では,診断当初無治療経過観察可能だったのは31例で,生存期間中央値は未達であった1)。MCL 8,029例の解析でdeferred therapy(診断日から90日を超えて治療開始)群492例と残りの7,537例を比較したところ,deferred therapy群が予後良好で,deferred therapyがOSの独立した予後因子であった2)。結果的に経過観察可能であった患者の予後は良好であることが示唆された。経過観察可能な患者の臨床的な特徴を検討したMCL 440例の解析では,診断から3カ月以上治療を行わなかった75例は,PS良好(0/1),B症状なし,LDH低値,non-bulky,芽球様バリアント以外,Ki-67<30%が有意に多かった。また,治療開始までの期間(time to treatment:TTT)中央値は35カ月で,TTTと有意に関連する因子として,non-nodalが同定された3)。MCLの予後不良因子とされるTP53変異を有する例においても18〜20カ月経過観察が可能であったとの報告もあり4),経過観察可能かの判断には臨床的な要素も重要である。WHO分類(2017)の「leukemic,non-nodal MCL」は,免疫グロブリン重鎖可変領域の遺伝子再構成頻度が通常のMCLとは異なる亜型で,SOX11陰性,病変部位は末梢血,骨髄,脾臓が中心でリンパ節腫大が軽度,進行が緩徐で通常のMCLより予後良好な病型である5)。
以上より,診断時に無治療経過観察可能な症例を正確に鑑別することは困難であるが,臨床経過が緩徐である場合,無治療経過観察も選択肢になる。
参考文献
1) Martin P, et al. Outcome of deferred initial therapy in mantle-cell lymphoma. J Clin Oncol. 2009; 27(8): 1209-13.(3iiiA)
2) Cohen JB, et al. Deferred therapy is associated with improved overall survival in patients with newly diagnosed mantle cell lymphoma. Cancer. 2016; 122(15): 2356-63.(3iiiA)
3) Abrisqueta P, et al. Observation as the initial management strategy in patients with mantle cell lymphoma. Ann Oncol. 2017; 28(10): 2489-95.(3iA)
4) Kumar A, et al. Clinical presentation determines selection of patients for initial observation in mantle cell lymphoma. Haematologica. 2019; 104(4): e163-6.(3iiiA)
5) Swerdiow SH, et al. Mantle cell lymphoma. Swedlow SH, et al. eds. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC; 2017: pp-285-90.
CQ3 若年初発進行期MCLにどのような治療が勧められるか
- 推奨グレード
- カテゴリー1
若年初発進行期MCLには,リツキシマブと大量シタラビン療法を含んだ導入療法を施行し,奏効例に自家移植併用大量化学療法による地固め療法とリツキシマブ維持療法を実施することが推奨される。
解説
若年MCLに対するCHOP類似レジメンで初回寛解達成後,地固め療法としての自家移植の有効性を検証する前方視的試験において,自家移植はインターフェロン群に比べてPFSを延長させ,有用性が示された1)。後方視的ながら,大規模コホート研究において,寛解導入後の地固め療法としての自家移植はPFSの延長をもたらすことが示されている2)。
自家移植前の導入化学療法として,リツキシマブ(R)併用化学療法に大量シタラビン(AraC)療法を組み入れた寛解導入療法がMCLの予後を改善するかを検証した第Ⅲ相試験の結果,R-CHOP療法とR-DHAP療法を交互に3コースずつ実施する大量AraC群は,R-CHOP療法6コース群に比べて,主要評価項目の治療不成功までの期間を有意に延長し,PFSも延長した3)。OSに関しては,大量AraC療法は,OSを延長する傾向にあったが,有意差は認められなかったものの,大量AraC療法を含んだ導入化学療法が標準治療と結論された。
自家移植前の導入化学療法として,R-maxi-CHOP療法(R,CPA,DXR,VCR,PSL)/R-HD-AraC療法(R,大量AraC)4),RB(R,BEN)/RC(R,AraC)療法5,6),本邦からはR-high-CHOP/CHASER療法(CPA,大量AraC,DEX,ETP,R)7)が報告されており,同等の治療成績が示されている。より有用な自家移植前導入療法を選択するために実施されたR-hyper-CVAD/MA交替療法(R,CPA,VCR,DXR,DEX,大量MTX,大量AraC)とBR療法とのランダム化比較第Ⅱ相試験では,R-hyper-CVAD/MA交替療法はBR療法に比べて,有害事象の頻度が高く,幹細胞採取効率が不良であることが示されている8)。
自家移植後にR維持療法を実施することで,PFSのみならずOSが延長することが報告されている9)。ただし,維持療法を3年間実施する設定であり,本邦の承認期間である2年間を適応した場合の有用性は明らかではない。
導入化学療法+維持療法にブルトンキナーゼ(BTK)阻害薬イブルチニブを併用することで治療成績が改善した臨床試験の結果が示されているが,本邦では適用外である。
以上より,若年初発進行期MCLには,Rと大量AraC療法を含んだ導入療法を施行し,奏効例に自家移植併用大量化学療法による地固め療法とR維持療法を実施することが推奨される。
参考文献
1) Dreyling M, et al. Early consolidation by myeloablative radiochemotherapy followed by autologous stem cell transplantation in first remission significantly prolongs progression-free survival in mantle-cell lymphoma: results of a prospective randomized trial of the European MCL Network. Blood. 2005; 105(7): 2677-84.(3iiiDiii)
2) Gerson JN, et al. Survival Outcomes of Younger Patients With Mantle Cell Lymphoma Treated in the Rituximab Era. J Clin Oncol. 2019; 37(6): 471-80.(3iiiDiii)
3) Hermine O, et al. Addition of high-dose cytarabine to immunochemotherapy before autologous stem-cell transplantation in patients aged 65 years or younger with mantle cell lymphoma(MCL Younger): a randomised, open-label, phase 3 trial of the European Mantle Cell Lymphoma Network. Lancet. 2016; 388(10044): 565-75.(1ii)
4) Eskelund CW, et al. 15-year follow-up of the Second Nordic Mantle Cell Lymphoma trial(MCL2): prolonged remissions without survival plateau. Br J Haematol. 2016; 175(3): 410-8.(3iiiDiii)
5) Armand P, et al. A phase 2 study of Rituximab-Bendamustine and Rituximab-Cytarabine for transplant-eligible patients with mantle cell lymphoma. Br J Haematol. 2016; 173(1): 89-95.(3iiiDiv)
6) Merryman RW, et al. Rituximab/bendamustine and rituximab/cytarabine induction therapy for transplant-eligible mantle cell lymphoma. Blood Adv. 2020; 4(5): 858-67.(3iiiDiv)
7) Ogura M, et al. R-High-CHOP/CHASER/LEED with autologous stem cell transplantation in newly diagnosed mantle cell lymphoma: JCOG0406 STUDY. Cancer Sci. 2018; 109(9): 2830-40.(3iiiDiii)
8) Chen RW, et al. RB but not R-HCVAD is a feasible induction regimen prior to auto-HCT in frontline MCL: results of SWOG Study S1106. Br J Haematol. 2017; 176(5): 759-69.(3iiiDiii)
9) Le Gouill S, et al. Rituximab after Autologous Stem-Cell Transplantation in Mantle-Cell Lymphoma. N Engl J Med. 2017; 377(13): 1250-60.(1iiDi)
10)Dreyling, M et al. Ibrutinib combined with immunochemotherapy with or without autologous stem-cell transplantation versus immunochemotherapy and autologous stem-cell transplantation in previously untreated patients with mantle cell lymphoma (TRIANGLE): a three-arm, randomised, open-label, phase 3 superiority trial of the European Mantle Cell Lymphoma Network. Lancet 2024; 403(10441): 2293-306.(1iiDi)
CQ4 高齢者(66歳以上),あるいは若年者(65歳以下)でも強力化学療法の適応とならない初発進行期MCLに対してどのような治療が勧められるか
- 推奨グレード
- カテゴリー2A
BR療法,R-CHOP療法,VR-CAP療法、I+BRが推奨される。R-CHOP療法奏効例には,リツキシマブ維持療法追加でOSが改善するため推奨される。
解説
60歳以上のMCLを対象にR-FC療法(R,FLU,CPA)とR-CHOP療法(R,CPA,DXR,VCR,PSL)を比較した第Ⅲ相試験では,奏効率(ORR),完全奏効率(CRR)で有意差は認めなかったが,4年OSはR-CHOP群62%,R-FC群47%で,R-CHOP群が上回った。また,リツキシマブ(R)維持療法は有意に再発もしくは死亡リスクを減少させた1)。この試験のR投与期間は病勢増悪までであり,本邦の承認期間とは異なる点に留意が必要である。VR-CAP療法(BOR,R,CPA,DXR,PSL)とR-CHOP療法の比較試験では,ORRはほぼ同等であったが2),PFS中央値はVR-CAP群24.7カ月,R-CHOP群14.4カ月,OS中央値はVR-CAP群90.7カ月,R-CHOP群55.7カ月で,いずれもVR-CAP療法が有意に上回った3)。VR-CAP療法後の維持療法のエビデンスはない。BR療法(BEN,R)とR-CHOP療法の第Ⅲ相試験におけるMCLのサブグループ解析では,BR療法が有意にPFSを延長した4)。BR療法とR-CHOP/R-CVP療法の比較試験におけるMCLの副次的解析でも,BR療法がPFSを有意に延長した5)。BR療法とBR療法にイブルチニブを上乗せした(I+BR)療法との比較試験の結果,イブルチニブを上乗せすることによりPFS中央値の延長が示されたが,OSでは有意差がなかった6)。I+BR療法群は,再発は少なかったが,有害事象死亡が多かった。
以上より,移植非適応初発MCLに対してR-CHOP療法,BR療法,VR-CAP療法,I+BR療法が選択肢となり,R-CHOP療法奏効例に対してR維持療法追加が有用である。
参考文献
1) Kluin-Nelemans HC, et al. Treatment of older patients with mantle-cell lymphoma. N Engl J Med. 2012; 367(6): 520-31.(1iiDiv)
2) Robak T, et al. Bortezomib-based therapy for newly diagnosed mantle-cell lymphoma. N Engle J Med. 2015; 372(10): 944-53.(1iiDiii)
3) Robak T, et al. Frontline bortezomib, rituximab, cyclophosphamide, doxorubicin, and prednisone(VR-CAP)versus rituximab, cyclophosphamide, doxorubicin, vincristine, and prednisone(R-CHOP)in transplantation-ineligible patients with newly diagnosed mantle cell lymphoma: final overall survival results of a randomised, open-label, phase 3 study. Lancet Oncol. 2018; 19(11): 1449-58.(1iiA)
4) Rummel MJ, et al. Bendamustine plus rituximab versus CHOP plus rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: an open-label, multicentre, randomised, phase 3 non-inferiority trial. Lancet. 2013; 381(9873): 1203-10.(1iiDiii)
5) Flinn IW, et al. First-Line Treatment of Patients With Indolent Non-Hodgkin Lymphoma or Mantle-Cell Lymphoma With Bendamustine Plus Rituximab Versus R-CHOP or R-CVP: Results of the BRIGHT 5-Year Follow-Up Study. J Clin Oncol. 2019; 37(12): 984-91.(1iiDiv)
6)Wang ML, et al. Ibrutinib plus Bendamustine and Rituximab in Untreated Mantle-Cell Lymphoma. N Engl J Med. 2022; 386(26): 2482-2494.(1iDiii)
CQ5 初発進行期MCLに対してリツキシマブ維持療法を実施すべきか
- 推奨グレード
- カテゴリー1
自家移植後,また移植非適応でR-CHOP療法を実施した場合には,リツキシマブ維持療法を実施することが推奨されるが,最適な投与期間は不明である。
解説
若年進行期MCLに対する自家移植後のリツキシマブ(R)維持療法の有用性に関する後方視的解析では,一定の結果が認められていなかった1-6)。しかしながら,18〜65歳の自家移植適応の初発MCL 299例に対して実施された第Ⅲ相比較試験の結果,2カ月ごと3年間のR維持療法により,若年者MCLのOSを延長することが示されたことから,自家移植後のR維持療法は標準治療と考えられる7)。メタアナリシスからも,未治療移植適応MCLに対してR併用化学療法による導入療法とそれに引き続く自家移植後のR維持療法は,PFSおよびOSを改善することが確認されている8)。ただし,上記第Ⅲ相比較試験でのR維持療法の期間は3年であり,本邦での承認期間である2カ月ごと12回2年とは異なることに留意が必要である。
年齢が65歳以上および自家移植非適応患者を対象とした高齢MCLにおいて,R-CHOP療法(R,CPA,DXR,VCR,PSL)を実施した後にR維持療法を行うことで,PSFおよびOSが延長することが示されている9,10)。ただし,この試験おけるR投与期間も,病勢増悪まで継続であるため,本邦の承認期間とは異なる点は留意が必要である。BR療法後のR維持療法の有用性に関しての一定したエビデンスは存在しない。
以上から,自家移植後,また移植非適応でR-CHOP療法を実施した場合には,R維持療法を実施することが推奨されるが,最適な投与期間は不明である。
参考文献
1) Mei MG, et al. Long-Term Results of High-Dose Therapy and Autologous Stem Cell Transplantation for Mantle Cell Lymphoma: Effectiveness of Maintenance Rituximab. Biol Blood Marrow Transplant. 2017; 23(11): 1861-9.(3iiiA)
2) Graf SA, et al. Maintenance rituximab after autologous stem cell transplantation in patients with mantle cell lymphoma. Ann Oncol. 2015; 26(11): 2323-8.(3iiiA)
3) Ahmadi T, et al. Potential prolongation of PFS in mantle cell lymphoma after R-HyperCVAD: auto-SCT consolidation or rituximab maintenance. Bone Marrow Transplant. 2012; 47(8): 1082-6.(3iiiA)
4) Falcone U, et al. Effectiveness and tolerability of first-line autologous stem cell transplant and maintenance rituximab for mantle cell lymphoma. Bone Marrow Transplant. 2018; 53(3): 347-51.(3iiiA)
5) Dietrich S, et al. Rituximab maintenance therapy after autologous stem cell transplantation prolongs progression-free survival in patients with mantle cell lymphoma. Leukemia. 2014; 28(3): 708-9.(3iiiA)
6) Klener P, et al. Rituximab maintenance significantly prolongs progression-free survival of patients with newly diagnosed mantle cell lymphoma treated with the Nordic MCL2 protocol and autologous stem cell transplantation. Am J Hematol. 2019; 94(2): E50-3.(3iiA)
7) Le Gouill S, et al. Rituximab after Autologous Stem-Cell Transplantation in Mantle-Cell Lymphoma. N Engl J Med. 2017; 377(13): 1250-60.(1iiDi)
8) Hilal T, et al. Rituximab maintenance therapy for mantle cell lymphoma: A systematic review and meta-analysis. Am J Hematol. 2018; 93(10): 1220-6.
9) Kluin-Nelemans HC, et al. Treatment of older patients with mantle-cell lymphoma. N Engl J Med. 2012; 367(6): 520-31.(1iiDiv)
10)Kluin-Nelemans HC, et al. Treatment of Older Patients With Mantle Cell Lymphoma(MCL): Long-Term Follow-Up of the Randomized European MCL Elderly Trial. J Clin Oncol. 2020; 38(3): 248-56.(1iiDiv)
CQ6 再発・難治性MCLに対してどのような治療が勧められるか
- 推奨グレード
- カテゴリー2B
再発・難治性MCLに対して,イブルチニブ,ピルトブルチニブ,ベンダムスチン,ボルテゾミブ単剤あるいはリツキシマブとの併用,GDP療法などの多剤併用療法が推奨される。
解説
再発・難治性MCLを対象としたブルトンキナーゼ(BTK)阻害薬イブルチニブ(IBT)の第Ⅱ相試験では,ORR 68%,CRR 21%1),24カ月時点のPFS 31%,OS 47%であった2)。下痢,出血傾向などの有害事象は,治療開始6カ月間の頻度が高く,以降は減少した2)。BTK阻害薬の前治療歴のある再発・難治性MCLを対象とした非共有型BTK阻害薬ピルトブルチニブ(PRT)の第Ⅰ/Ⅱ相試験では,ORR 57.8%,CRR 20%,DOR中央値21.6カ月,PFS中央値7.4カ月であった3)。また,本邦適用外ではあるが,ベネトクラクス(VEN)4),リツキシマブ(R)の併用5)で良好な成績が報告されている。BR療法(BEN,R)の第Ⅱ相試験では,ORR 82%,CRR 40%であった6)。BR療法とFR療法(R,FLU)の比較試験のMCLの副次的解析では,BR療法はPFSを延長した7)。R-BAC療法(R,BEN,AraC)ではORR 80%であった8)。ボルテゾミブ(BOR)の治療効果は単剤でORR 33%9),R,デキサメタゾン(DEX)との併用でORR 81.3%であった10)。救援療法として汎用されているGDP療法(Gem,DEX,CDDP)あるいはGD療法(Gem,DEX)も一定の治療効果が確認されている11)。救援療法不応例では臨床試験への参加も選択肢となる。
以上より,再発・難治性MCLに対する標準治療は確立しておらず,前治療の使用薬剤,奏効持続期間を考慮して,IBT,PRT,BEN,BOR単剤あるいはRとの併用,GDP療法などの多剤併用療法が推奨される。
参考文献
1)Wang ML, et al. Targeting BTK with ibrutinib in relapsed or refractory mantle-cell lymphoma. N Engl J Med. 2013; 369(6): 507-16.(3iiiDiv)
2)Wang ML, et al. Long-term follow-up of MCL patients treated with single-agent ibrutinib: updated safety and efficacy results. Blood. 2015; 126(6): 739-45.(3iiiDiv)
3)Wang ML, et al. Pirtobrutinib in Covalent Bruton Tyrosine Kinase Inhibitor Pretreated Mantle-Cell Lymphoma. J Clin Oncol.2023; 41(24): 3988-3997.(3iiiDiv)
4)Tam CS, et al. Ibrutinib plus Venetoclax for the Treatment of Mantle-Cell Lymphoma. N Engl J Med. 2018; 378(13): 1211-23.(3iiiDiv)
5)Wang ML, et al. Ibrutinib in combination with rituximab in relapsed or refractory mantle cell lymphoma: a single-centre, open-label, phase 2 trial. Lancet Oncol. 2016; 17(1): 48-56.(3iiiDiv)
6)Czuczman MS, et al. Phase II study of bendamustine combined with rituximab in relapsed/refractory mantle cell lymphoma: efficacy, tolerability, and safety findings. Ann Hematol. 2015; 94(12): 2025-32. (3iiiDiv)
7)Rummel M, et al. Bendamustine plus rituximab versus fludarabine plus rituximab for patients with relapsed indolent and mantle-cell lymphomas: a multicentre, randomised, open-label, non-inferiority phase 3 trial. Lancet Oncol. 2016; 17(1): 57-66.(1iiDiii)
8)Visco C, et al. Combination of rituximab, bendamustine, and cytarabine for patients with mantle-cell non-Hodgkin lymphoma ineligible for intensive regimens or autologous transplantation. J Clin Oncol. 2013; 31(11): 1442-9.(3Div)
9)Fisher RI, et al. Multicenter phase II study of bortezomib in patients with relapsed or refractory mantle cell lymphoma. J Clin Oncol. 2006; 24(30): 4867-74.(3iiiDiv)
10)Lamm W, et al. Bortezomib combined with rituximab and dexamethasone is an active regimen for patients with relapsed and chemotherapy-refractory mantle cell lymphoma. Haematologica. 2011; 96(7): 1008-14.(3iiiDiv)
11)Morschhauser F, et al. Phase II study of gemcitabine-dexamethasone with or without cisplatin in relapsed or refractory mantle cell lymphoma. Ann Oncol. 2007; 18(2): 370-5.(3iiiDiv)
CQ7 再発・難治性MCLに対して同種移植の適応はあるか
- 推奨グレード
- カテゴリー2B
再発・難治性MCLに対して,現時点で同種移植は治療選択肢の一つである。
解説
リツキシマブ(R)導入前,後において,再発・難治性MCLに対する同種移植の成績に関する報告があるが,すべて後方視的解析であり,前方視的比較試験はない。
再発・難治性MCLに対して,同種移植を実施することにより,生存曲線の平坦化が認められ,化学療法抵抗性でも一定の割合(25%)で移植後持続的寛解を達成し得ること1),また,TP53変異を有する予後不良なMCL2)や移植前残存病変陽性例でも長期予後を改善し得る3)ことから,治療戦略の一つと考えられる。しかしながら,非再発死亡による早期死亡が多いことには注意が必要である。
本邦でのTRUMPに登録された症例解析では,同種移植例において高いNRMであった反面,再発率は3年で18.3%と低かった。また,3年PFSは54.3%であった4)。
以上から,再発・難治性MCLに対して同種移植は治療選択肢の一つとなり得る。
参考文献
1) Hamadani M, et al. Allogeneic hematopoietic cell transplantation for chemotherapy-unresponsive mantle cell lymphoma: a cohort analysis from the center for international blood and marrow transplant research. Biol Blood Marrow Transplant. 2013; 19(4): 625-31.(3iDiii)
2) Lin RJ, et al. Allogeneic haematopoietic cell transplantation impacts on outcomes of mantle cell lymphoma with TP53 alterations. Br J Haematol. 2019; 184(6): 1006-10.(3iiiDiii)
3) Magnusson E, et al. Hematopoietic cell transplantation for mantle cell lymphoma: predictive value of pretransplant positron emission tomography/computed tomography and bone marrow evaluations for outcomes. Clin Lymphoma Myeloma Leuk. 2014; 14(2): 114-21.(3iiiDiv)
4) Yamasaki S, et al. Impact of hematopoietic stem cell transplantation in patients with relapsed or refractory mantle cell lymphoma. Ann Hematol. 2018; 97(8): 1445-52.(3iDiv)

